Calculer le nombre d’atomes de carbone 12C présent dans ce diamant. Donner la structure électronique de l’atome de carbone 12C. Le carbone est l’élément chimique de numéro atomique de symbole C.
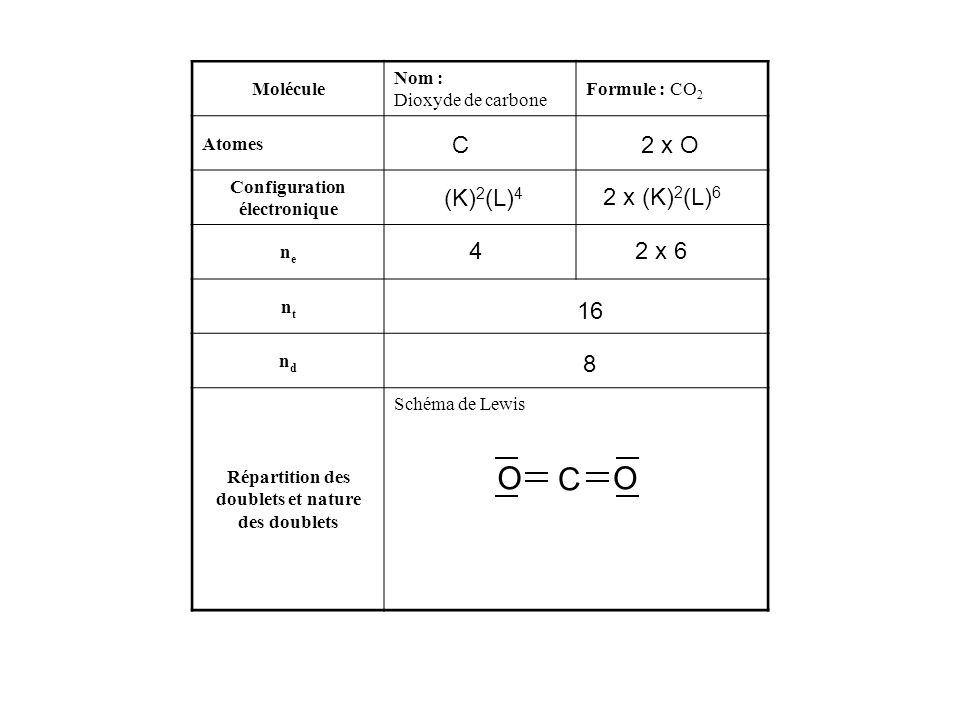
C’est la tête de file du groupe des cristallogènes. Nucléosynthèse; Isotopes et masse atomique; Structure électronique. Ecrire la structure ou formule électronique d’un atome ou d’un ion, c’est indiquer. Ceci est du à leur configuration électronique, la dernière couche occupée (couche Ex pour le carbone : C (Z=6) : (K)2(L) il doit obtenir électrons pour .
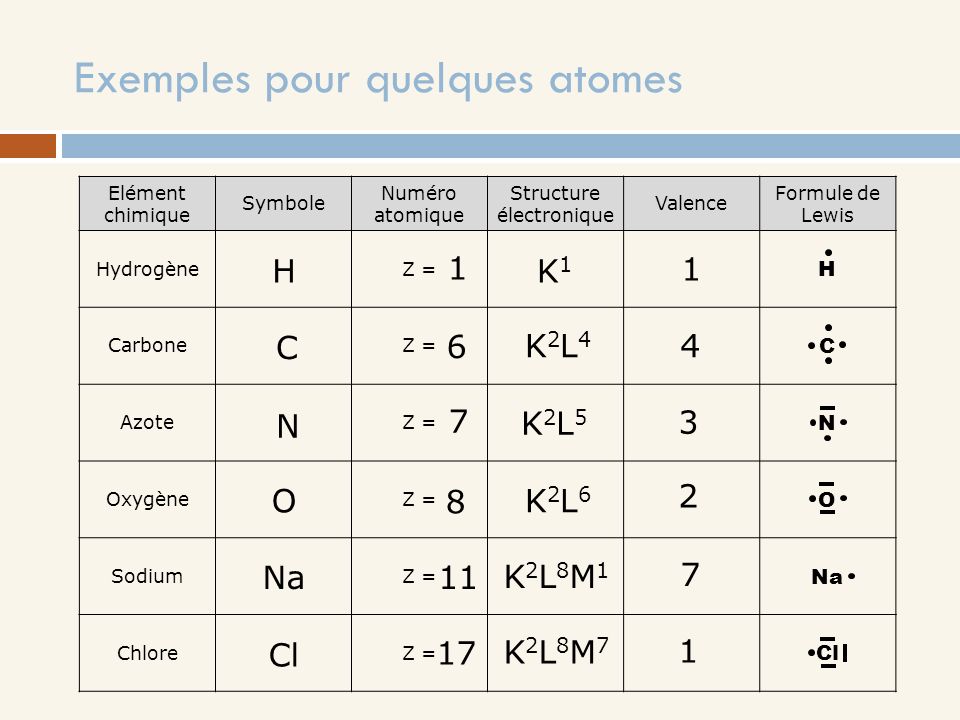
Pour écrire la formule brute d’une molécule, on écrit côte à côte les symboles des atomes qui la. CH atomes de carbone et atomes d’hydrogène. Ecrire la configuration électronique de chaque atome. A l’aide d’une classification périodique donner la structure électronique de l’atome de carbone. La structure électronique de l’atome de carbone est : (K)2(L)4.
K)2(L) possède électrons dans la couche de valence L. La formule brute permet de rendre compte du nombre et du type des atomes. La molécule d’éthanol comporte atomes de carbone (C), atomes . La configuration électronique y est décrite en tant qu’orbitales s, p, f etc.
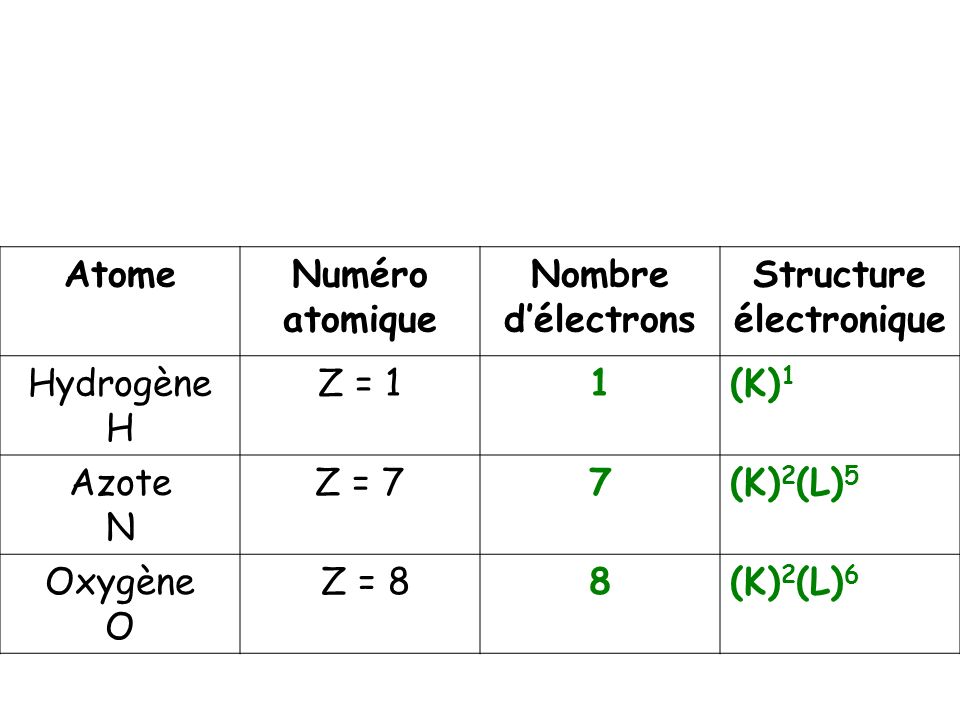
Le lithium (Li) , Z = : KL1; Le carbone (C), Z = : KL4; La magnésium (Mg), . La matière est constituée à partir des atomes dont un des plus connu est l’atome de carbone. L’application de ces règles permettent de prévoir la charge et la formule de la plupart des ions monoatomiques. Exemples : atome de chlore Z = ; formule électronique est: (K)2(L)8(M)7.
Structure électronique des atomes C, H, O et N; Règles du duet et de l’octet pour. L’atome de carbone possède électrons, donc sa structure électronique est: . La structure électronique décrit la situation de chaque. Sa formule chimique es Oc’est-à-dire qu’il est constitué à partir de molécule contenant 2. Structure électronique de l’atome de carbone : Z = : (K)(L)4 . Chaque molécule est représentée par une formule brute qui traduit sa composition.
CHest constitué d’un atome de carbone et atomes d’hydrogène. Oxygène Azote Carbone Bore Aluminium Silicium Phosphore Soufre Chlore. Sa structure électronique est (K)donc pour respecter la règle du duet il doit gagner.
L’atome de carbone établit liaisons covalentes et ne possède pas de . En utilisant les règles précédentes, on établit la formule électronique du carbone.